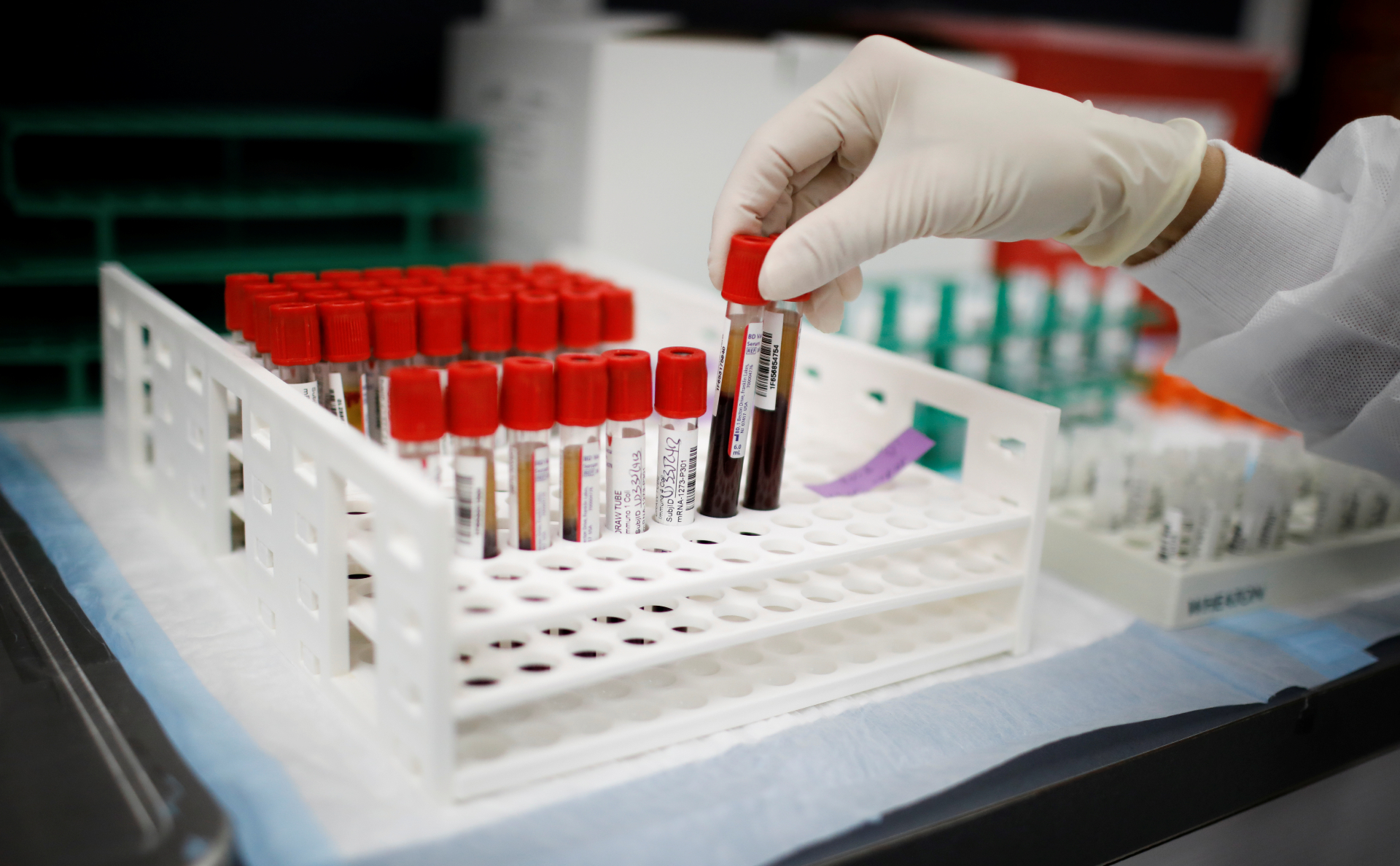
Шесть вопросов о российской вакцине от коронавируса: тесты, нюансы, риски
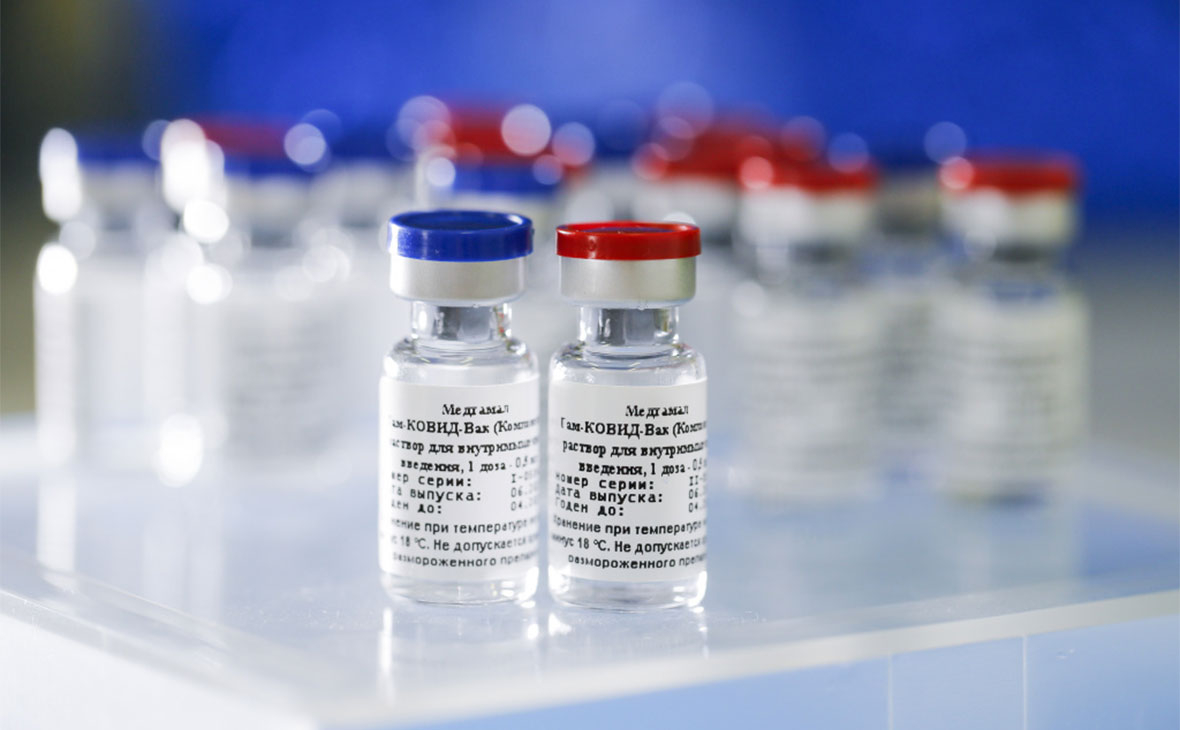
Кого будут прививать в первую очередь?
Первыми вакцину получат люди из группы риска: врачи, работники и учащиеся школ и вузов, призывники, полицейские. Затем — социальные работники, сотрудники транспорта и сферы услуг: банков, гостиниц, торговли и общепита. Дети и пожилые люди смогут прививаться, когда закончат испытания на пациентах их возраста.
Сейчас вакцина доступна для совершеннолетних граждан РФ, которые знают русский язык (чтобы заполнить все документы). Прививку можно делать спустя 30 дней после других прививок и как минимум через две недели после ОРВИ. Сначала нужно сдать анализы на антитела к коронавирусу. Если показатель IgG выше 10, прививка не нужна.
Массовая вакцинация для всех остальных начнется в 2021 году. Глава Центра им. Гамалеи Александр Гинцбург считает, что на всеобщую вакцинацию россиян уйдет до 12 месяцев. По его словам, если привить 70–80% населения, это остановит распространение коронавирусной инфекции в стране.
Что известно про вакцину?
«Спутник V» разрабатывали с февраля 2020 года в Национальном центре эпидемиологических и микробиологических исследований имени Н.Ф.Гамалеи Минздрава России. Еще в процессе первых испытаний создатели заявили, что у вакцины нет серьезных побочных эффектов. Разработкой и испытаниями руководил Денис Логунов, который до этого разрабатывал вакцины против Эболы и MERS.
При создании нового препарата он фактически скопировал вакцину MERS.
«Спутник V» относится к векторным вакцинам: в их основе — аденовирус человека. В его геноме содержится вставка, которая кодирует фрагмент S-белка вируса SARS-CoV-2 и вызывает иммунный ответ организма.
Вакцина состоит из двух компонентов (векторов) и вводится в два этапа с интервалом три недели. Двухвекторная вакцина помогает увеличить шансы: если первый вектор в течение двух недель не начнет воспроизводиться, колоть его снова бесполезно — иммунитет к вирусу будет слишком слабым. Но можно вколоть второй и получить нужную реакцию.
Вакцину намереваются выпускать уже как минимум три фармкомпании: «Р-фарм», «Генериум», «Биннофарм». К концу года планируют выпустить от 3 млн до 8 млн доз препарата.
Почему так быстро выдали регистрацию?
11 августа вакцину действительно зарегистрировали условно, еще до окончания финальной фазы испытаний. Минздрав РФ выдал временную регистрацию до 1 января 2021 года. Это сделали в соответствии с особым порядком доступа на рынок препаратов для профилактики COVID-19, принятым правительством.
Если при тестировании на большой выборке вакцина покажет негативные последствия, регистрацию могут отозвать. Но при положительном исходе препарат зарегистрируют на постоянной основе. Подобные же схемы сейчас применяют и в других странах, пострадавших от коронавируса, например в Великобритании и США.
Что не так с испытаниями?
На момент регистрации «Спутник V» прошел две стадии испытаний, в каждой из которых участвовали по 38 добровольцев. У всех выработались высокие титры антител — это значит, что иммунный ответ на вакцину был хорошим. Критики сомневаются в достоверности результатов: каждой группе давали разные версии препаратов — высушенную и обычную (замороженную), поэтому сравнивать их некорректно.
Третья стадия еще не завершена. В ней должны принять участие 40 тыс. человек. Часть из них получат два вектора вакцины, остальные — плацебо.
В начале сентября создатели вакцины опубликовали статью в журнале The Lancet, где описали результаты I и II фазы испытаний. Однако вскоре опубликованные данные вызвали споры.
Сначала Матти Сэльберг, глава отделения лабораторной медицины Каролинского института, заявил, что выборка слишком мала и по ней нельзя однозначно судить об эффективности и безопасности препарата. К тому же генномодифицированные вирусы еще очень слабо изучены, а предыдущие подобные разработки китайских медиков были неудачными. Так что последствия от их применения сложно предсказать.
В начале августа сервис «Справочник врача» опросил более 3 тыс. российских медиков. Из них на вакцинацию согласились только 24,5%, а 52% высказались против. Более 66% усомнились в том, что опубликованных данных достаточно, чтобы судить об эффективности «Спутника V». Среди обычных россиян против прививки выступают 73%.
Затем группа более чем из 40 ученых-исследователей (включая российских) опубликовала открытое письмо в адрес редакции The Lancet и авторов публикации о вакцине. Им показалось странным, что графики уровня антител у испытуемых разных групп в разные дни слишком похожи. Чтобы проверить данные, авторы письма просили опубликовать исходные цифры и показания приборов.
Разработчики вакцины ответили публикацией в том же журнале. Они утверждают, что данные приведены в исходном виде. Все совпадения случайны и связаны с тем, что исследования проводили среди очень небольшого количества людей. Почему выборка была такой узкой — так и не объяснили и никаких новых данных не предоставили.
Этот ответ не удовлетворил авторов письма: вероятность случайного совпадения в таких исследованиях составляет чуть больше 1%. Поэтому вопрос о корректности испытаний остался открытым.
Среди других претензий — то, что в первых двух фазах не применяли плацебо, а испытания проводили на молодых людях с хорошим иммунитетом. При этом от коронавируса больше всего страдают пожилые и ослабленные люди с хроническими заболеваниями сердца и сосудов. К тому же данные об испытаниях опубликовали до того, как прошло 180 дней, — минимальный срок для выявления всех побочных эффектов. Некоторые специалисты отмечают, что иммунитет после российской вакцины сопоставим с иммунитетом переболевших коронавирусом, а этого явно недостаточно.
По данным Русской службы BBC, когда проводили III фазу испытаний, некоторые добровольцы даже были не в курсе, что участвуют в тестировании. Их направляли руководители бюджетных организаций под видом обычной вакцинации, причем в обязательном порядке. О том, что они могут получить плацебо, тоже подозревали далеко не все.
Вакцина может быть опасна?
Этого мы точно не узнаем, пока не завершат все испытания и наблюдения. Но создатели вакцины утверждают, что постарались свести риски к минимуму.
Во-первых, выбрали именно векторный, а не инактивированный тип. Это значит, что вакцина содержит измененный кусок безопасного для человека вируса со специальной программой в геноме. Инактивированные вакцины содержат вирус целиком, специально выращенный и убитый. Такие препараты чаще вызывают ADE-эффект (англ. antibody-dependent enhancement, антителозависимое усиление инфекции): когда введение вакцины вызывает размножение вируса в организме.
Векторные вакцины в отличие от инактивированных вызывают не только реакцию антител, но и цитотоксическую: появляются иммунные клетки, которые прицельно уничтожают вирусные.
Во-вторых, вакцину сделали двухвекторной: сначала один вектор, а потом второй. Так вирус не успеет размножиться и причинить вред.
По словам создателей, пока побочные эффекты от вакцины похожи на легкую простуду: повышение температуры, головная боль, слабость, насморк — то есть самые типичные.
Жизнь и здоровье добровольцев, которые участвуют в испытаниях, застрахованы. Если в результате вакцинации они получат травмы и заболевания, им выплатят от 300 тыс. до 1,5 млн руб., в зависимости от тяжести. В случае их гибели родственники получат 2 млн руб.
До сих пор неясно, насколько опасной может быть вакцина для пожилых, людей с хроническими заболеваниями и аллергиков: их в числе испытуемых не было.
А что там с другими вакцинами?
Россия первой зарегистрировала вакцину, но испытания ведутся во многих странах. В гонке участвуют 35 лабораторий по всему миру и более 170 вакцин.
Главные претенденты — китайские и американские препараты от разных лабораторий. В основном это те же векторные вакцины, но уже с одним вектором. Создатели вакцины из Оксфордского университета и AstraZenecа тоже опубликовали предварительные результаты испытаний, приложив все исходные данные.
Для вакцин против COVID-19 за рубежом тоже действуют ускоренные правила регистрации, согласно рекомендациям ВОЗ. Однако испытания этих препаратов проходят дольше, чем в России, так как исследования проводят на большем числе добровольцев.
В России же на днях зарегистрируют новую вакцину — «ЭпиВакКорона» от центра «Вектор». Она прошла все фазы испытания 30 сентября. В РАН говорят, что никаких нежелательных симптомов у участников исследования пока не выявили. Еще один препарат разрабатывают в Центре им. Чумакова: он недавно получил разрешение на испытания от Минздрава.